
Minimální vzorec, jak získat minimální vzorec, příklady a cvičení
The minimální nebo empirický vzorec Je to vyjádření podílu, ve kterém jsou přítomny atomy různých prvků, které tvoří chemickou sloučeninu. Minimální vzorec je tedy nejjednodušší reprezentací chemické sloučeniny. Proto je „minimální“.
Minimální vzorec nevyjadřuje počty atomů různých prvků, které tvoří chemickou sloučeninu; ale poměr, ve kterém se tyto atomy spojí a vytvoří chemickou sloučeninu.
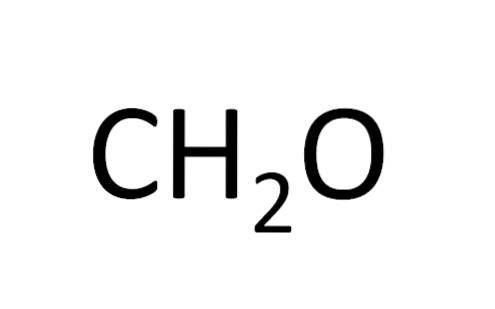
Minimální vzorec se také nazývá empirický vzorec, protože je získán experimentováním; to znamená, že to souvisí se zkušeností. Experimentální pozorování umožnilo dospět k závěru, že dva atomy vodíku se spojí s jedním atomem vodíku za vzniku vody (HdvaNEBO).
V mnoha případech se minimální vzorec shoduje s molekulárním vzorcem. V molekule se objevují reálná čísla různých prvků, které tvoří chemickou sloučeninu; tak je tomu například v případě kyseliny sírové (HdvaSW4).
Ale v jiných případech neexistuje shoda minimálního vzorce a molekulárního vzorce; To je případ benzenu: minimální vzorec je CH, zatímco jeho molekulární vzorec je C6H6.
Rejstřík článků
- 1 Jak získat minimální vzorec?
- 1.1 První krok
- 1.2 Druhý krok
- 1.3 Třetí krok
- 1.4 Čtvrtý krok
- 2 Příklady minimálního vzorce
- 2.1 Voda a oxid uhličitý
- 2.2 Zásadité a kyselé oxidy
- 2.3 Kyselina octová
- 2.4 Kyselina máselná
- 2.5 Ethylenglykol
- 2.6 Benzen
- 2.7 Glukóza
- 3 Vyřešená cvičení
- 3.1 - Cvičení 1
- 3.2 - Cvičení 2
- 4 Odkazy
Jak získat minimální vzorec?
První krok
Najděte gramy každého prvku přítomného ve sloučenině. Protože jsou obvykle vyjádřeny jako procento hmotnosti sloučeniny, musí být proveden jednoduchý výpočet pro transformaci hmotnostních procent v hmotnosti prvků.
Druhý krok
Získá se relativní počet atomů různých prvků, které tvoří chemickou sloučeninu. K tomu je hmotnost každého prvku, vyjádřená v gramech, vydělena atomovou hmotností.
Někteří autoři raději nazývají relativní počet atomů jako počet molů atomů prvků, které jsou součástí chemické sloučeniny.
Třetí krok
Získání minimálního podílu, vyjádřeného v celých číslech, každého z atomů přítomných v chemické sloučenině.
Chcete-li najít tyto hodnoty, vydělte relativní počet každého atomu přítomného ve sloučenině minimální relativní číselnou hodnotou, kterou má atom v chemické sloučenině..
V případě, že hodnota minimálního podílu atomu není celé číslo bez desetinných míst, musí být všechny hodnoty minimálního podílu vynásobeny číslem; takovým způsobem, že umožňuje, aby všechny hodnoty minimálního poměru byly celá čísla.
Například pokud je hodnota minimálního podílu atomu chemické sloučeniny 2,5, vynásobte každý hodnoty minimálního podílu každého z atomů v současné době 2. Všechny hodnoty minimálního podílu tedy budou pouze celá čísla.
Čtvrtý krok
Napište minimální vzorec sloučeniny. Hodnoty minimálního podílu atomů různých prvků budou umístěny jako dolní indexy chemických symbolů prvků k napsání minimálního vzorce.
Minimální příklady vzorců
Voda a oxid uhličitý
Většina chemických sloučenin má vzorce, které jsou jak minimální, tak molekulární. Vzorec pro vodu (HdvaO) je minimální vzorec; ale je to také molekulární vzorec. Totéž platí pro vzorec pro oxid uhličitý (COdva).
Oxidy zásadité a kyselé
Zásadité a kyselé oxidy jsou chemické sloučeniny, které mají chemické vzorce, až na několik výjimek, které jsou minimální i molekulární. Stejná situace nastává u hydroxidů a kyselin, s výjimkou některých karboxylových kyselin..
Octová kyselina
Karboxylové kyseliny, které mají ve svém složení sudý počet atomů uhlíku, mají odděleně minimální vzorec a molekulární vzorec. Například kyselina octová má molekulární vzorec (CdvaH4NEBOdva); ale má také minimální vzorec (CHdvaNEBO).
Kyselina máselná
Kyselina máselná má také molekulární vzorec (C4H8NEBOdva) a minimální vzorec (C.dvaH4NEBO).
Ethylenglykol
Jiné organické sloučeniny mají oba typy chemických vzorců; takový je případ ethylenglykolu, který má molekulární vzorec (C.dvaH6NEBOdva) a minimální vzorec (CH3NEBO).
Benzen
Benzen, aromatická sloučenina, má molekulární vzorec (C.6H6) a minimální vzorec (CH).
Glukóza
Glukóza má molekulární vzorec (C.6H12NEBO6) a minimální vzorec (CHdvaNEBO).
Vyřešená cvičení
- Cvičení 1
Ethylenglykol je sloučenina používaná jako nemrznoucí směs, má molekulovou hmotnost 62,1 g / mol a hmotnostní procentní složení takto:
C: 38%,
H: 9,7%
Nebo: 51,16%.
První krok
Vyjádřete hmotnostní procenta prvků v jejich hmotnostech v gramech. Z tohoto důvodu se jako reference bere molekulová hmotnost ethylenglykolu. Pokud je to 62,1 gramů na mol, 38% z toho tvoří uhlík. A tak dále s dalšími prvky:
Uhlíková hmotnost = 62,1 g (38/100)
= 23,6 g
Hmotnost vodíku = 62,1 g (9,7 / 100)
= 6,024 g
Hmotnost kyslíku = 62,1 g (51,16 / 100)
= 31,77 g
Druhý krok
Vypočítejte relativní počet každého přítomného atomu (NRA) nebo počet molů každého atomu. Za tímto účelem se hmotnost každého chemického prvku vydělí jeho atomovou hmotou.
NRA (C) = 23,6 g / 12 g
= 1,97
Lze zaokrouhlit na 2.
NRA (H) = 6,024 g / 1 g
= 6,024
Může být zaokrouhleno na 6.
NRA (O) = 31,77 g / 16 g
= 1985
Lze zaokrouhlit na 2.
Třetí krok
Vypočítejte minimální celočíselný poměr prvků sloučeniny (PMNE). Chcete-li to provést, vydělte každou z hodnot atomových relativních čísel (NRA) nejmenší hodnotou. V tomto případě 2.
PMNE (C) = 2/2
= 1
PMNE (H) = 6/2
= 3
PMNE (O) = 2/2
= 1
Čtvrtý krok
Napište minimální vzorec pro ethylenglykol:
CH3NEBO
Jak je možné vidět, hodnoty získané v kroku 3 jsou indexy prvků sloučeniny.
- Cvičení 2
Kyselina octová má molekulovou hmotnost 60 g / mol a následující hmotnostní procentní složení:
C: 40%
H: 6,67%
Nebo: 53,33%
Získejte minimální vzorec sloučeniny.
První krok
Transformujte hmotnostní procenta prvků na jejich hmotnosti vyjádřené v gramech:
Uhlíková hmota = 60 g (40/100)
= 24 g
Hmotnost vodíku = 60 g (6,67 / 100)
= 4 g
Hmotnost kyslíku = 60 g (53,33 / 100)
= 32 g
Druhý krok
Vypočítejte relativní počet atomů (NRA) sloučeniny. Za tímto účelem se hmotnosti prvků dělí jejich atomovými hmotnostmi:
NRA (C) = 24 g / 12 g
= 2
NRA (H) = 4 g / 1 g
= 4
NRA (O) = 32 g / 16 g
= 2
Třetí krok
Získejte minimální poměr celých čísel prvků sloučeniny (PMNE). Za tímto účelem se hodnoty NRA prvků vydělí nejnižší hodnotou NRA, kterou má prvek:
PMNE (C) = 2/2
= 1
PMNE (H) = 4/2
= 2
PMNE (O) = 2/2
= 1
Čtvrtý krok
Napište minimální vzorec pro kyselinu octovou:
CHdvaNEBO
Dolní indexy sloučeniny jsou hodnoty získané z PMNE.
Reference
- Whitten, Davis, Peck a Stanley. (2008). Chemie. (8. vydání). Učení CENGAGE.
- Helmenstine, Anne Marie, Ph.D. (27. srpna 2019). Empirický vzorec: Definice a příklady. Obnoveno z: thoughtco.com
- Wikipedia. (2020). Empirický vzorec. Obnoveno z: en.wikipedia.org
- Chemistry LibreTexts. (3. července 2019). Výpočet empirických vzorců pro sloučeniny. Obnoveno z: chem.libretexts.org
- Nicola McDougal. (2020). Empirický vzorec: definice, kroky a příklady. Studie. Obnoveno z: study.com


Zatím žádné komentáře