
Vlastnosti, struktura, funkce Laccase
The domy, p-Difenol: dioxygen oxidoreduktázy nebo benzendiol-kyslík oxidoreduktázy, jsou enzymy, které patří do skupiny oxidázových enzymů nazývaných „oxidázy modré mědi“.
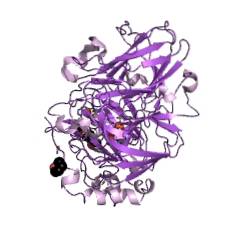
Existují ve vyšších rostlinách, v některých hmyzích, v bakteriích a prakticky ve všech studovaných houbách; jeho charakteristická modrá barva je produktem čtyř atomů mědi připojených k molekule v jejím katalytickém místě.
Tyto enzymy popsal Yoshida a spolupracovníci v roce 1883, když studovali pryskyřici stromu Rhus vernicifera nebo japonský „lakovaný strom“, kde bylo stanoveno, že jeho hlavní funkcí je katalyzovat polymerační a depolymerační reakce sloučenin..
Mnohem později bylo zjištěno, že u hub tyto proteiny s enzymatickou aktivitou mají specifické funkce v mechanismech odstraňování toxických fenolů z prostředí, kde rostou, zatímco v rostlinách se účastní syntetických procesů, jako je lignifikace.
Vědecké pokroky týkající se studia těchto enzymů umožnily jejich použití na průmyslové úrovni, kde byla využita jejich katalytická kapacita, zejména v kontextech bioremediace, textilu, při odstraňování barviv aplikovaných na textil, v papírenském průmyslu, mimo jiné.
Hlavní důvody, proč jsou lakcasy z průmyslového hlediska tak zajímavé, souvisí se skutečností, že jejich oxidační reakce jednoduše zahrnují redukci molekulárního kyslíku a produkci vody jako sekundárního prvku..
Rejstřík článků
- 1 Funkce
- 1.1 Distribuce
- 1.2 Katalýza
- 2 Struktura
- 2.1 Isoenzymy
- 3 funkce
- 3.1 V rostlinách
- 3.2 V houbách
- 3.3 V průmyslu
- 4 Odkazy
Vlastnosti
Enzymy lakcase mohou být vylučovány nebo nalezeny v intracelulární oblasti, ale to záleží na studovaném organismu. Navzdory tomu většina analyzovaných enzymů (s výjimkou některých proteinů z určitých hub a hmyzu) jsou extracelulární proteiny..
Rozdělení
Jak bylo diskutováno výše, tyto enzymy se nacházejí převážně v houbách, vyšších rostlinách, bakteriích a některých druzích hmyzu..
Mezi rostlinami, kde se prokázala jeho existence, jsou jabloně, chřest, brambory, hrušky, mango, broskve, borovice, švestky a další. Hmyz vyjadřující lakázu patří hlavně k rodům Bombyx, Calliphora, Diploptera, Drosophila, Musca, Papilio, Rhodnius, a další.
Houby jsou organismy, ze kterých bylo izolováno a studováno největší množství a rozmanitost lazarů, a tyto enzymy jsou přítomny jak v ascomycetách, tak v deuteromycetách a basidiomycetách..
Katalýza
Reakce katalyzovaná lakalázami spočívá v monoelektronické oxidaci molekuly substrátu, která může patřit do skupiny fenolů, aromatických sloučenin nebo alifatických aminů, na odpovídající reaktivní radikál.
Výsledkem katalytické reakce je redukce jedné molekuly kyslíku na dvě molekuly vody a současně oxidace čtyř molekul substrátu za vzniku čtyř reaktivních volných radikálů..
Meziproduktové volné radikály se mohou vázat a tvořit dimery, oligomery nebo polymery, a proto se říká, že lakazy katalyzují polymerační a „depolymerační“ reakce..
Struktura
Lakcasy jsou glykoproteiny, to znamená, že se jedná o proteiny, které mají oligosacharidové zbytky kovalentně navázané na polypeptidový řetězec a tyto představují mezi 10 a 50% z celkové hmotnosti molekuly (v rostlinných enzymech může být procento o něco vyšší).
Sacharidová část tohoto typu proteinu obsahuje monosacharidy, jako je glukóza, manóza, galaktóza, fukóza, arabinóza a některé hexosaminy, a předpokládá se, že glykosylace hraje důležitou roli při sekreci, proteolytické citlivosti, aktivitě, retenci mědi a tepelné stabilitě protein.
Obecně se tyto enzymy v přírodě nacházejí jako monomery nebo homodimery a molekulová hmotnost každého monomeru se může pohybovat mezi 60 a 100 kDa.
Katalytické centrum laccases je tvořeno čtyřmi atomy mědi (Cu), které dávají molekule obecně modrou barvu díky elektronické absorpci, která probíhá ve vazbách měď-měď (Cu-Cu)..
Rostlinné lakcasy mají izoelektrické body s hodnotami blízkými 9 (zcela zásadní), zatímco fungální enzymy jsou mezi izoelektrickými body 3 a 7 (jsou to tedy enzymy, které pracují v kyselých podmínkách).
Isoenzymy
Mnoho hub produkujících lakázu má také izoformy lakázy, které jsou kódovány stejným genem nebo různými geny. Tyto izoenzymy se od sebe liší hlavně svou stabilitou, optimálním pH a teplotou katalyzující a svou afinitou k různým typům substrátu..
Za určitých podmínek mohou mít tyto izoenzymy různé fyziologické funkce, ale záleží to na druhu nebo stavu, ve kterém obývá..
Funkce
Někteří vědci prokázali, že se lakazy podílejí na „sklerotizaci“ kutikuly u hmyzu a na hromadění spor odolných vůči ultrafialovému záření v mikroorganismech rodu Bacil.
V rostlinách
V rostlinných organismech se lakcasy podílejí na tvorbě buněčné stěny, na procesech lignifikace a „delignifikace“ (ztráta nebo rozpad ligninu); a navíc souvisí s detoxikací tkání oxidací antifungálních fenolů nebo deaktivací fytoalexinů.
V houbách
Významně hojné v této skupině organismů se lakcasy účastní různých buněčných a fyziologických procesů. Mezi nimi lze zmínit ochranu patogenních hub tříslovin a rostlinných „fytoalexinů“; lze tedy říci, že pro houby jsou tyto enzymy faktory virulence.
Lakcasy mají také funkce v morfogenezi a diferenciaci struktur rezistence a spor bazidiomycetů, jakož i v biodegradaci ligninu v plísních, které degradují tkáně dřevin..
Lakázy se současně podílejí na tvorbě pigmentů v myceliích a plodnicích mnoha hub a přispívají k procesům adheze buněk k buňkám, při tvorbě polyfenolického „lepidla“, které váže hyfy, a při vyhýbání se imunitě. systém hostitelů infikovaných patogenními houbami.
V průmyslu
Tyto konkrétní enzymy se průmyslově používají pro různé účely, ale ty nejvýznamnější odpovídají textilnímu a papírenskému průmyslu a bioremediaci a dekontaminaci odpadních vod produkovaných jinými průmyslovými procesy..
Konkrétně se tyto enzymy často používají k oxidaci fenolů a jejich derivátů přítomných ve vodě kontaminované průmyslovým odpadem, jehož produkty katalýzy jsou nerozpustné (polymerované) a sraženiny, což je činí snadno oddělitelnými..
V potravinářském průmyslu mají také určitý význam, protože odstranění fenolových sloučenin je nezbytné pro stabilizaci nápojů, jako je víno, pivo a přírodní džusy..
Používají se v kosmetickém průmyslu, při chemické syntéze mnoha sloučenin, při bioremediaci půdy a v nanobiotechnologii.
Nejpoužívanější jsou lakázy z hub, ale v poslední době bylo zjištěno, že bakteriální lakáza má z průmyslového hlediska výraznější vlastnosti; Jsou schopné pracovat s větší škálou substrátů a při mnohem širším rozmezí teplot a pH, navíc jsou mnohem stabilnější proti inhibičním látkám.
Reference
- Claus, H. (2004). Lakázy: struktura, reakce, distribuce. Mikron, 35, 93-96.
- Couto, S. R., Luis, J., & Herrera, T. (2006). Průmyslové a biotechnologické aplikace laccases: recenze. Biotechnologické pokroky, 24, 500-513.
- Madhavi, V. a Lele, S. S. (2009). Laccase: vlastnosti a aplikace. Biozdroje, 4(4), 1694-1717.
- Riva, S., Molecolare, R., & Bianco, V. M. (2006). Lakcases: modré enzymy pro zelenou chemii. Trendy v biotechnologii, 24(5), 219-226.
- Singh, P., Bindi, C., & Arunika, G. (2017). Bakteriální lakáza: poslední aktualizace týkající se výroby, vlastností a průmyslových aplikací. Biotech, 7(323), 1-20.

Zatím žádné komentáře