
Chirality, z čeho se skládá, a příklady
The chirality Jedná se o geometrickou vlastnost, ve které může mít objekt dva obrazy: jeden pravý a jeden levý, které nejsou zaměnitelné; to znamená, že jsou prostorově odlišné, i když zbytek jejich vlastností je totožný. O objektu vykazujícím chirality se jednoduše říká, že je ‚chirální '.
Pravá a levá ruka jsou chirální: jedna je odrazem (zrcadlovým obrazem) druhé, ale nejsou stejné, protože při umístění jedné na druhou se jejich palce neshodují.
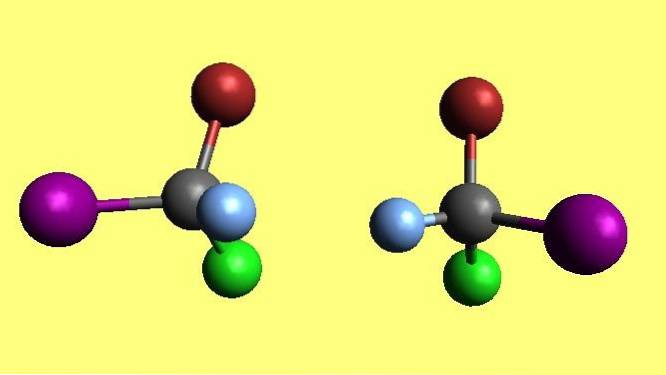
Více než zrcadlo, abyste věděli, zda je objekt chirální, je třeba si položit následující otázku: má „verze“ pro levou i pravou stranu?
Například levák a pravák jsou chirální předměty; dvě vozidla stejného modelu, ale s volantem vlevo nebo vpravo; boty, stejně jako nohy; točitá schodiště doleva, doprava, atd..
A v chemii nejsou molekuly výjimkou: mohou být také chirální. Obrázek ukazuje dvojici molekul s čtyřboká geometrie. I když je ten nalevo převrácený a modrá a fialová koule se dotýkají, hnědé a zelené koule „vypadají“ z letadla..
Rejstřík článků
- 1 Co je chirality?
- 2 Příklady chirality
- 2.1 Axiální
- 2.2 Rovinný
- 2.3 Ostatní
- 3 Odkazy
Co je chiralita?
U molekul není tak snadné určit, která je levá nebo pravá „verze“ pouhým pohledem na ně. Za tímto účelem se organičtí chemici uchylují k konfiguracím Cahn-Ingold-Prelog® nebo (S) nebo v optické vlastnosti těchto chirálních látek k rotaci polarizovaného světla (což je také chirální prvek)..
Není však těžké určit, zda je molekula nebo sloučenina chirální, pouhým pohledem na její strukturu. Jaký je výrazný rys dvojice molekul na horním obrázku??
Má čtyři různé substituenty, každý s vlastní charakteristickou barvou, a také geometrie kolem centrálního atomu je čtyřstěnná..
Pokud ve struktuře existuje atom se čtyřmi různými substituenty, lze konstatovat (ve většině případů), že molekula je chirální.
Pak se říká, že ve struktuře je centrum chirality nebo stereogenní centrum. Tam, kde je jeden, bude pár stereoizomerů známých jako enantiomery.
Dvě molekuly na obrázku jsou enantiomery. Čím větší je počet chirálních center, které sloučenina vlastní, tím větší je její prostorová rozmanitost..
Centrální atom je obecně atom uhlíku ve všech biomolekulách a sloučeninách s farmakologickou aktivitou; může to však být také fosfor, dusík nebo kov.
Příklady chirality
Centrum chirality je možná jedním z nejdůležitějších prvků při určování, zda je sloučenina chirální nebo ne..
Existují však i další faktory, které mohou zůstat nepovšimnuté, ale u 3D modelů odhalují zrcadlový obraz, který nelze překrývat..
U těchto struktur se pak říká, že místo středu mají jiné prvky chirality. S ohledem na to již přítomnost asymetrického centra se čtyřmi substituenty nestačí, ale je třeba pečlivě analyzovat i zbytek struktury; a být tak schopen odlišit jeden stereoizomer od druhého.
Axiální

Sloučeniny uvedené výše se mohou pouhým okem jevit jako ploché, ale ve skutečnosti tomu tak není. Nalevo je obecná struktura allenu, kde R označuje čtyři různé substituenty; a na pravé straně obecná struktura bifenylové sloučeniny.
Extrém, kde se R. setkávají3 a R.4 lze zobrazit jako „ploutev“ kolmo k rovině, kde leží R1 a R.dva.
Pokud pozorovatel analyzuje takové molekuly umístěním oka před první uhlík vázaný na R.1 a R.dva (pro alene), uvidíte R.1 a R.dva na levou a pravou stranu a na R4 a R.3 nahoru a dolů.
Pokud R3 a R.4 zůstávají pevné, ale jsou změněny R1 napravo a Rdva vlevo bude další „prostorová verze“.
Zde může pozorovatel dojít k závěru, že pro Allena našel osu chirality; totéž se děje s bifenylem, ale s aromatickými kruhy zapojenými do vidění.
Kroužkové šrouby nebo Helicity
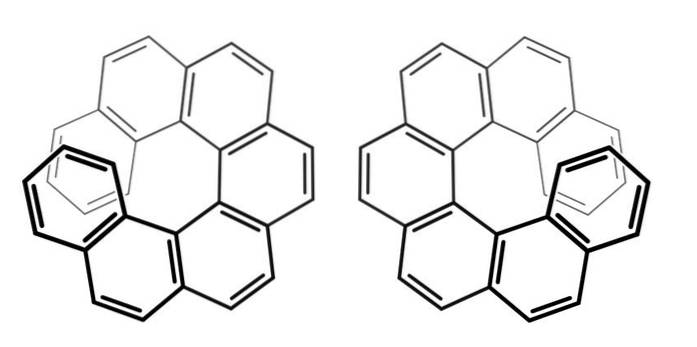
Všimněte si, že v předchozím příkladu ležela osa chirality v kostře C = C = C pro allen a ve vazbě Ar-Ar pro bifenyl.
Jaká je jejich osa chirality pro výše uvedené sloučeniny nazývané heptahelceny (protože mají sedm kruhů)? Odpověď je uvedena na stejném obrázku výše: osa Z, osa vrtule.
Proto, abyste rozeznali jeden enantiomer od druhého, musíte se na tyto molekuly podívat shora (nejlépe).
Tímto způsobem lze popsat, že se heptahelicen otáčí ve směru hodinových ručiček (levá strana obrázku) nebo proti směru hodinových ručiček (pravá strana obrázku)..
Rovinný
Předpokládejme, že už nemáte helicen, ale molekulu s nekoplanárními prstenci; to znamená, že jeden je umístěn nad nebo pod druhým (nebo nejsou ve stejné rovině).
Zde chirální znak nespočívá tolik na kruhu, ale na jeho substituentech; to jsou ty, které definují každý ze dvou enantiomerů.

Například ve ferrocenu na horním obrázku se prstence, které „sendvičují“ atom Fe, nemění; ale prostorová orientace kruhu s atomem dusíku a skupinou -N (CH3)dva.
Na obrázku je skupina -N (CH3)dva ukazuje doleva, ale ve svém enantiomeru bude ukazovat doprava.
Ostatní
U makromolekul nebo u singulárních struktur se obraz začíná zjednodušovat. Proč? Protože z jejich 3D modelů je možné z ptačí perspektivy vidět, zda jsou či nejsou chirální, jak se to děje u objektů v počátečních příkladech..
Například uhlíková nanotrubice může ukazovat vzory zatáček doleva, a proto je chirální, pokud existuje stejná, ale se zatáčkami doprava..
Totéž se děje s jinými strukturami, kde, i když nemají centra chirality, může mít prostorové uspořádání všech jejich atomů chirální formy..
Mluvíme tedy o inherentní chirality, která nezávisí na atomu, ale na celé množině..
Chemicky silný způsob rozlišení „levého obrazu“ od pravého je stereoselektivní reakcí; tj. ten, kde se může vyskytovat pouze u jednoho enantiomeru, zatímco u druhého č.
Reference
- Carey F. (2008). Organická chemie. (Šesté vydání). Mc Graw Hill.
- Wikipedia. (2018). Chirality (chemie). Obnoveno z: en.wikipedia.org
- Advameg, Inc. (2018). Chirality. Obnoveno z: chemistryexplained.com
- Steven A. Hardinger a Harcourt Brace & Company. (2000). Stereochemie: Stanovení molekulární chirality. Obnoveno z: chem.ucla.edu
- Harvardská Univerzita. (2018). Molekulární chirality. Obnoveno z: rowland.harvard.edu
- Oregonská státní univerzita. (14. července 2009). Chirality: chirální a achirální objekty. Obnoveno z: science.oregonstate.edu



Zatím žádné komentáře