
Struktura, funkce a související patologie titiny
Titina je termín používaný k popisu dvojice obrovských polypeptidových řetězců, které tvoří třetí nejhojnější protein v sarkomérech širokého spektra kosterních a srdečních svalů.
Titin je jedním z největších známých proteinů z hlediska počtu aminokyselinových zbytků, a tedy z hlediska molekulové hmotnosti. Tento protein je také známý jako připojit a je přítomen u obratlovců i bezobratlých.
Poprvé byl s tímto názvem (connectin) popsán v roce 1977 a v roce 1979 byl definován jako dvojitý pás v horní části polyakrylamidového gelového elektroforetického gelu za denaturačních podmínek (s dodecylsulfátem sodným). V roce 1989 byla jeho poloha stanovena imunoelektronovou mikroskopií.
Spolu s dalším velkým proteinem, nebulinem, je titin jednou z hlavních složek elastické sítě cytoskeletu svalových buněk, která koexistuje se silnými vlákny (myosin) a tenkými vlákny (aktin) v sarkomerech; natolik, že je známý jako třetí vláknový systém svalových vláken.
Silná a tenká vlákna jsou zodpovědná za generování aktivní síly, zatímco titinová vlákna určují viskoelasticitu sarkomér.
Sarkoméra je opakující se jednotka myofibril (svalová vlákna). Je přibližně 2 μm dlouhý a je ohraničen „deskami“ nebo řádky zvanými Z řádky, které segmentují každý myofibril do pruhovaných fragmentů definované velikosti.
Molekuly titinu se skládají do extrémně dlouhých, pružných, tenkých a roztažitelných vláknitých vláken. Titin je zodpovědný za pružnost kosterního svalu a předpokládá se, že funguje jako molekulární lešení, které určuje správné sestavení sarkomér v myofibrilách..
Rejstřík článků
- 1 Struktura
- 2 funkce
- 2.1 Další funkce
- 3 Související patologie
- 4 Odkazy
Struktura
U obratlovců má titin přibližně 27 000 aminokyselinových zbytků a molekulovou hmotnost přibližně 3 MDa (3 000 kDa). Skládá se ze dvou polypeptidových řetězců známých jako T1 a T2, které mají podobné chemické složení a podobné antigenní vlastnosti..
Ve svalu bezobratlých jsou „mini-titiny„Mezi 0,7 a 1,2 MDa molekulové hmotnosti. Tato skupina proteinů zahrnuje protein "Twitchina" z Caenorhabditis elegans a bílkoviny "Projectin" nalezený v žánru Drosophila.
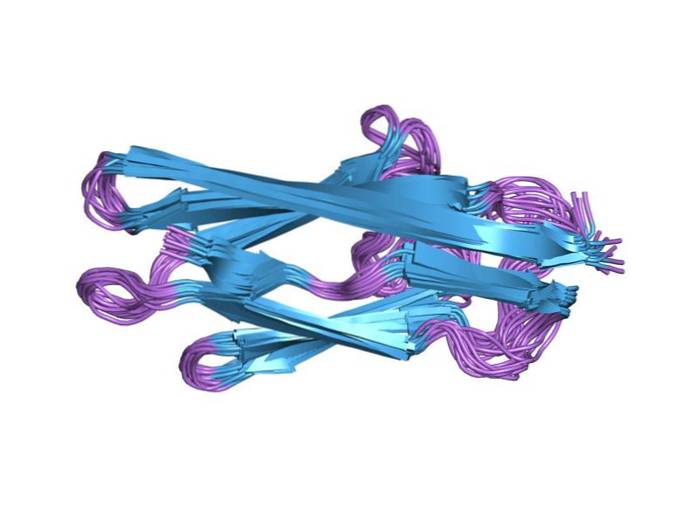
Titan obratlovců je modulární protein složený převážně z domén podobných imunoglobulinu a fibronektinu III (FNIII-jako) uspořádány v dávce. Má elastickou oblast bohatou na prolin, kyselinu glutamovou, valinové a lysinové zbytky známé jako doména PEVK a další doménu serinkinázy na svém karboxylovém terminálním konci..
Každá z domén je dlouhá přibližně 100 aminokyselin a je známá jako titin třídy I (doména III podobná fibronektinu) a titin třídy II (doména podobná imunoglobulinu). Obě domény se skládají do 4 nm dlouhých „sendvičových“ struktur složených z antiparalelních p-listů..
Srdeční molekula pro připojení obsahuje 132 opakujících se motivů imunoglobulinové domény a 112 opakujících se motivů domény podobné fibronektinu III..
Kódující gen pro tyto proteiny (TTN) je „šampionem“ intronů, protože jich má uvnitř téměř 180.
Transkripty podjednotek jsou odlišně zpracovávány, zejména kódující oblasti imunoglobulinových (Ig) a PEVK podobných domén, které vedou k izoformám s různými rozšiřitelnými vlastnostmi..
Funkce
Funkce titinu v sarkomérech závisí na jeho asociaci s různými strukturami: jeho C-terminální konec je ukotven k M linii, zatímco N-terminální konec každého titinu je ukotven k Z linii.
Nebulinové a titinové proteiny fungují jako „molekulární vládci“, které regulují délku silných a tenkých vláken. Titin, jak již bylo zmíněno, sahá od disku Z až za linii M ve středu sarkomery a reguluje jeho délku, čímž brání přetažení svalového vlákna..
Ukázalo se, že skládání a rozkládání titinu napomáhá procesu svalové kontrakce, to znamená, že vytváří mechanickou práci, při které se dosahuje zkrácení nebo prodloužení sarkomér; zatímco tlustá a tenká vlákna jsou molekulárními motory pohybu.
Titin se podílí na údržbě tlustých vláken ve středu sarkomery a jeho vlákna jsou odpovědná za generování pasivního napětí během protahování sarkomér..
Další funkce
Kromě své účasti na tvorbě viskoelastické síly má titin další funkce, mezi které patří:
-Účast na mechanicko-chemických signalizačních událostech prostřednictvím její asociace s jinými sarkomerními a nesarkomerními proteiny
-Na délce závislá aktivace kontraktilního aparátu
-Sestava sarkomery
-Příspěvek ke struktuře a funkci cytoskeletu u obratlovců, mimo jiné.
Některé studie ukázaly, že v lidských buňkách a embryích Drosophila, titin má další funkci jako chromozomální protein. Elastické vlastnosti purifikovaného proteinu dokonale odpovídají elastickým vlastnostem chromozomů jak živých buněk, tak shromážděných chromozomů. in vitro.
Účast tohoto proteinu na zhutňování chromozomů byla prokázána díky místně zaměřeným experimentům s mutagenezí genu, který jej kóduje, což má za následek svalové i chromozomální defekty..
Lange a kol. V roce 2005 prokázali, že doména titinkinázy má co do činění s komplexním expresním systémem svalových genů, což dokazuje mutace této domény, která způsobuje dědičné svalové onemocnění.
Související patologie
Některá onemocnění srdce jsou spojena se změnami pružnosti titinu. Takové změny výrazně ovlivňují roztažnost a pasivní diastolickou tuhost myokardu a pravděpodobně mechanosenzitivitu..
Gen TTN byl identifikován jako jeden z hlavních genů podílejících se na lidských onemocněních, takže vlastnosti a funkce srdečního proteinu byly v posledních letech rozsáhle studovány.
Dilatovaná kardiomyopatie a hypertrofická kardiomyopatie jsou také produktem mutace několika genů, včetně genu TTN.
Reference
- Despopoulos, A., & Silbernagl, S. (2003). Barevný atlas fyziologie (5. vydání). New York: Thieme.
- Herman, D., Lam, L., Taylor, M., Wang, L., Teekakirikul, P., Christodoulou, D.,… Seidman, C. E. (2012). Zkrácení titinu způsobující dilatační kardiomyopatii. The New England Journal of Medicine, 366(7), 619-628.
- Keller, T. (1995). Struktura a funkce titinu a nebulinu. Aktuální názor v biologii, 7, 32-38.
- Lange, S., Lange, S., Xiang, F., Yakovenko, A., Vihola, A., Hackman, P.,… Gautel, M. (2005). Kinázová doména titinu řídí expresi svalového genu a přeměnu bílkovin. Věda, 1599-1603.
- Linke, W. A. a Hamdani, N. (2014). Gigantické podnikání: Vlastnosti a funkce titinu v tlustém a tenkém stavu. Výzkum oběhu, 114, 1052-1068.
- Machado, C., a Andrew, D. J. (2000). D-TITIN: Obří protein s dvojí rolí v chromozomech a svalech. The Journal of Cell Biology, 151(3), 639-651.
- Marujama, K. (1997). Obří elastický protein svalu. FASEB Journal, jedenáct, 341-345.
- Nelson, D. L. a Cox, M. M. (2009). Lehningerovy principy biochemie. Edice Omega (5. vydání).
- Rivas-Pardo, J., Eckels, E., Popa, I., Kosuri, P., Linke, W., & Fernández, J. (2016). Work Done by Titin Protein Folding pomáhá svalové kontrakci. Zprávy buněk, 14, 1339-1347.
- Trinick, J. (1994). Titin a nebulin: proteinové vládce ve svalech? Trendy v biochemických vědách, 19, 405-410.
- Tskhovrebova, L., & Trinick, J. (2003). Titin: Vlastnosti a rodinné vztahy. Recenze přírody, 4, 679-6889.
- Wang, K., Ramirez-Mitchell, R., & Palter, D. (1984). Titin je mimořádně dlouhý, flexibilní a štíhlý myofibrilární protein. Proc. Natl. Acad. Sci., 81, 3685-3689.


Zatím žádné komentáře